Ventilação Mecânica Protetora: Da Fisiopatologia à Monitorização Avançada à Beira-Leito
A ventilação mecânica (VM) é, reconhecidamente, a intervenção mais central da terapia intensiva moderna. Com cerca de 45 a 50 mil leitos de UTI adulto no Brasil, estima-se que em qualquer momento, 40% a 60% desses pacientes estejam sob suporte ventilatório. No entanto, o que deveria ser uma medida salvadora pode se tornar uma fonte de lesão se não for aplicada com rigor técnico e fisiológico.
Este artigo detalha os mecanismos de lesão, a evolução dos parâmetros protetores e as tecnologias que estão transformando o manejo da Síndrome do Desconforto Respiratório Agudo (SARA).
1. Mecanismos de Lesão Pulmonar Induzida pelo Ventilador (VILI)
Para proteger o pulmão, é fundamental entender como ele é lesionado. O conceito de VILI (Ventilator-Induced Lung Injury) define que pressões e volumes inadequados geram danos estruturais e inflamatórios.
- Volutrauma: Identificado na década de 70, refere-se à lesão por excesso de volume, levando à inundação alveolar por exsudato inflamatório.
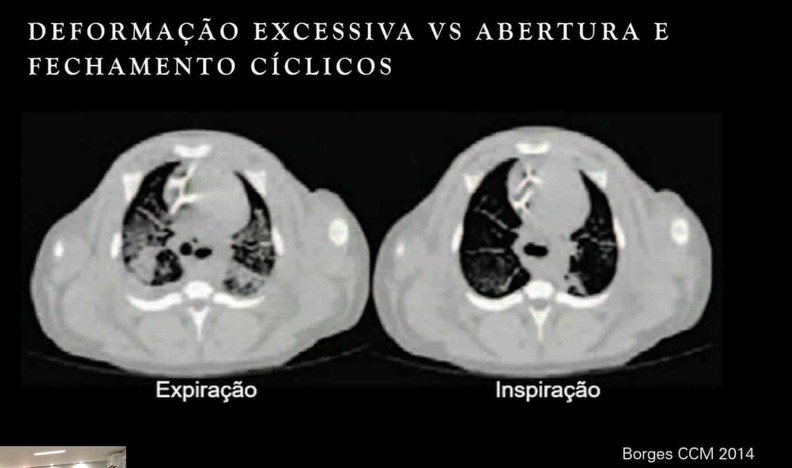
- Atelectrauma: Ocorre quando pressões expiratórias (PEEP) muito baixas permitem o colapso e a reabertura cíclica de alvéolos, gerando estresse mecânico.
- Biotrauma: A deformação celular excessiva libera citocinas (como IL-8) na circulação, explicando por que a lesão pulmonar pode causar falência múltipla de órgãos, como rins e intestino.
- Baby Lung: Na SARA, o volume de pulmão aerado é drasticamente reduzido, assemelhando-se ao tamanho do pulmão de uma criança. Esse “pulmão bebê” deve ser tratado com extrema gentileza.
2. A Revolução da Driving Pressure ()
Até meados de 2000, o foco era o volume corrente de 6 ml/kg (peso predito) e pressão de platô abaixo de 30 cmH2O. No entanto, em 2015, o grupo do Dr. Marcelo Amato demonstrou que a variável mais ligada à mortalidade é a Driving Pressure.
Por que a Driving Pressure é superior?
A fórmula reflete o volume corrente normalizado para a complacência (tamanho real do baby lung) do paciente. O estudo de Amato mostrou que:
- O aumento de 1 cmH2O na eleva a mortalidade em 4%.
- O alvo ideal deve ser abaixo de 15 cmH2O.
- A é o principal mediador do efeito de uma estratégia protetora, sendo mais fidedigna que o volume corrente isolado.
3. Monitorização Regional: Tomografia de Impedância Elétrica (TIE)
O ventilador oferece dados globais, mas o pulmão na SARA é heterogêneo. A TIE surge como um método não invasivo e contínuo que mede a resistência à corrente elétrica nos tecidos (impedância).
- Utilidade Clínica: Permite visualizar áreas de colapso (dorsais) e hiperdistensão (ventrais) em tempo real.
- Titulação de PEEP: Através do Método de Costa, identifica-se a “PEEP Ótima” — o ponto de cruzamento entre o menor colapso alveolar e a menor sobredistensão, garantindo a melhor complacência regional.
4. Pressão Transpulmonar e o Uso do Balão Esofágico
Muitas vezes, a pressão de platô mostrada no ventilador é influenciada pela caixa torácica (obesidade, ascite). O uso do balão esofágico permite estimar a pressão pleural e calcular a Pressão Transpulmonar ().
Para evitar o colapso, a inspiratória deve ser mantida em níveis seguros, enquanto a expiratória deve idealmente estar entre 0 e +3 cmH2O para garantir que os alvéolos permaneçam abertos ao final da expiração.
5. Estratégias Posicionais: Prona, Supina e Além
A posição prona não é apenas uma manobra de resgate para oxigenação; é uma estratégia de proteção que reduz o estresse e a deformação alveolar de forma mais homogênea.
- Recrutamento Sustentado: A associação de prona com PEEP individualizada acelera a recuperação pulmonar e reduz o tempo de VM.
- Mudanças de Decúbito: Estudos recentes indicam que mudanças laterais e ajustes no ângulo do tronco (30º-45º vs 0º) influenciam a mecânica respiratória, a eliminação de CO2 e podem até recrutar áreas pulmonares devido à histerese.
6. O Futuro: Ventilação Personalizada e IA
A tendência caminha para a automação inteligente. Ventiladores com Inteligência Artificial poderão detectar assincronias e ajustar parâmetros em tempo real com base no fenótipo pulmonar (focal vs. não focal). Como destacado na aula, o futuro não é usar mais tecnologia, mas usar a melhor fisiologia aliada à tecnologia.
——————————————————————————–
Referências Bibliográficas Selecionadas
- ARDS Definition Task Force. Acute Respiratory Distress Syndrome: The Berlin Definition. JAMA. 2012;307(23):2526-2533. (Referência para a classificação da SARA citada na aula).
- The Acute Respiratory Distress Syndrome Network (ARDSNet). Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. N Engl J Med. 2000;342:1301-1308. (Marco do uso de 6 ml/kg).
- Amato, M. B. P., et al. Driving pressure and survival in the acute respiratory distress syndrome. N Engl J Med. 2015;372(8):747-755. (Estudo fundamental sobre Driving Pressure).
- Gattinoni, L., & Pesenti, A. The concept of “baby lung”. Intensive Care Medicine. 2005;31(6):776-784. (Base para o manejo gentil do parênquima pulmonar).
- Borges, J. B., et al. Reversibility of lung collapse and hypoxemia in early acute respiratory distress syndrome. Am J Respir Crit Care Med. 2006;174(3):268-278. (Estudo sobre recrutamento alveolar mencionado pela palestrante).
- Costa, E. L., et al. Bedside estimation of recruitable lung collapse and hyperdistension by electrical impedance tomography. Intensive Care Medicine. 2009. (Referência para o Método de Costa na Tomografia de Impedância Elétrica).
- Cavalcanti, A. B., et al. (Writing Committee for the ART Investigators). Effect of Lung Recruitment and Titrated PEEP vs Low PEEP on Clinical Outcomes in Patients With Acute Respiratory Distress Syndrome: The ART Randomized Clinical Trial. JAMA. 2017;318(14):1335-1345. (Estudo ART sobre segurança nas manobras de recrutamento).
- Talmor, D., et al. Mechanical ventilation guided by esophageal pressure in acute respiratory distress syndrome (EPVent). N Engl J Med. 2008;359(20):2095-2104. (Referência para o uso do balão esofágico).
- Beitler, J. R., et al. Effect of titrating positive end-expiratory pressure (PEEP) with an esophageal pressure-guided strategy vs a low-PEEP strategy on death and days free from mechanical ventilation among patients with ARDS: the EPVent2 randomized clinical trial. JAMA. 2019;321(9):846-857..
- Gattinoni, L., et al. Effect of prone positioning on the survival of patients with acute respiratory failure. N Engl J Med. 2001;345(8):568-573. (Base científica para a estratégia de prona)